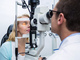
В статье рассмотрено влияние современных склеральных контактных линз на физиологию роговицы и ее слоев
- Введение
- Теоретический подход
- Клинические доказательства
- Ответ, затрагивающий всю структуру роговицы
- Механизмы компенсации
- Знаки гипоксии
- Другие клинические вопросы
- Уроки, полученные от применения мягких линз
- Можем ли мы улучшить ситуацию?
- Все сводится к балансу пользы и рисков
Введение
Современные склеральные линзы – это чудесная, восхитительная технология, обладающая потенциалом серьезно менять качество жизни человека. Рост рынка таких линз и числа специалистов, которые с ними работают в последнее время [1], показывает эффективность их применения для лечения ряда глазных заболеваний, восстановления зрительных функций роговиц с неправильной формой и коррекции простых аномалий рефракции у пациентов с обычной формой роговицы [2].
В то же время наше понимание действия склеральных линз эволюционировало в течение прошедшего десятилетия, и подход к их подбору постоянно пересматривается. Хотя многое остается неизвестным, ясно, что склеральные линзы могут порождать свойственные только им проблемы и осложнения [3] и для некоторых пациентов они просто не подходят. Например, у пациентов с кератоконусом при коррекции с помощью склеральных линз острота зрения может быть ниже оптимальной в силу аберраций высших порядков, вызываемых децентрированием линзы, по сравнению с использованием традиционных жестких газопроницаемых линз меньшего диаметра или гибридных линз [4]. У пациентов после пересадки роговицы наблюдается низкое число эндотелиальных клеток, точнее – низкое число здоровых эндотелиальных клеток, и это может рассматриваться как потенциальное противопоказание к ношению склеральных линз [5]. В таких случаях более подходящими будут меньшие по диаметру жесткие газопроницаемые линзы, хотя их подбор будет непростым.
Здесь мы подходим к дискуссии о транспорте кислорода к роговице через толщину склеральной линзы. В этой статье мы стремились свести воедино результаты теоретического моделирования и лабораторных исследований, она задает умеренный подход к подбору склеральных линз благодаря взвешиванию рисков и пользы для каждого пациента.
Теоретический подход
В 2012 году впервые была разработана теоретическая модель на основе критерия Харвитта–Бонанно (Harvitt–Bonanno) [6], а немного позднее – и математическая модель [7]. Обе модели дали понять, что склеральные линзы способны вызвать гипоксический стресс в центре роговицы в том случае, когда материал линзы имеет невысокую кислородную проницаемость, а также когда дизайн линзы предполагает увеличение ее толщины и объема подлинзового слезного резервуара. Авторы обеих моделей рекомендовали изготавливать склеральные линзы из материалов с высокой кислородной проницаемостью (Dk > 150), при этом максимальная толщина линзы должна быть не более 250 мкм, а глубина центрального слезного резервуара – не более 200 мкм.
Эти модели не подвергались сомнению в отношении их точности или научной ценности, но были заданы вопросы по поводу их клинической значимости [8], особенно в свете благоприятных исходов, которые регулярно отмечаются на практике, несмотря на неисполнение вышеназванных критериев [9, 10]. Некоторые из авторов исследований предположили, что при отсутствии явных клинических признаков любые связанные с гипоксией последствия будут минимальными; тем не менее для выбора правильной тактики требовалось проведение клинических исследований.
Клинические доказательства
Для определения наличия и клинического влияния гипоксического стресса на роговицу было важно основывать анализ на хорошо контролируемых исследованиях, а не на отзывах и случаях из практики.
Более современные исследования предоставили нам доказательства того, что ношение склеральных линз связано с гипоксическим стрессом, который проявляется как отек роговицы размером 1–3% на молодых здоровых глазах, в зависимости от дизайна линзы, материала, режима ношения. Большинство авторов этих исследований оценили уровень гипоксии как незлокачественный [11–14], сравнимый с уровнем отека, наблюдаемого после ночного сна или после ношения некоторых мягких гидрогелевых линз в течение дня, без значительных кратковременных побочных эффектов.
Такое сравнение может ввести в заблуждение). Несмотря на схожий уровень отека роговицы, физиологический отек обычно пропадает спустя 1 ч после пробуждения и открытия век, благодаря тому что роговица получает кислород из воздуха. Гипоксический же стресс, вызванный ношением склеральных линз, развивается быстро, за первые 45 мин [15], и сохраняется в течение всего времени ношения линз. В результате, если пациент надевает склеральные линзы после пробуждения, теоретически возможна ситуация, при которой роговица его глаз будет постоянно находиться в состоянии гипоксического стресса. В настоящее время у нас нет исследований долгосрочного эффекта незначительного отека роговицы, вызванного ношением склеральных линз, на здоровье роговицы и качество зрения.
Ответ, затрагивающий всю структуру роговицы
Одно из первых исследований in vitro, в котором изучалось ношение склеральных линз и вызванной им гипоксии, показало, что транспорт кислорода к роговой оболочке снижается на 30% на уровне эпителия при наличии слезного резервуара глубиной 400 мкм по сравнению с рекомендуемой его глубиной 200 мкм [16]. Это клиническое исследование подтвердило предыдущие теоретические модели и было поддержано другими клиническими работами, в которых было выявлено, что стромальный отек слегка увеличивается при увеличении глубины слезного резервуара (снижение транспорта кислорода на 25% при глубине резервуара 431 мкм по сравнению с 225 мкм) [15]. В этом исследовании развитие стромального отека происходило быстро, после чего по мере ношения линз он слегка уменьшился, но за 8 ч их использования так и не прошел. Основываясь на этих открытиях, авторы посчитали, что нужно подбирать склеральные линзы с минимальным подъемом задней поверхности над центром роговицы для того, чтобы снизить гипоксический стресс, в частности в случае скомпрометированных роговиц (низкое число эндотелиальных клеток) [16].
Недавно было проведено исследование in vivo, в котором показан значительный эндотелиальный ответ на гипоксический стресс, связанный с ношением склеральных контактных линз [17]. Наличие пузырьков, быстрое развитие роговичной гипоксии и ацидоза [18], которые являются транзиторными по природе, обнаруживались вскоре после надевания линз, и эти последствия были более сильно выражены в случае подбора линзы с глубоким резервуаром слезы под ней (400 мкм против рекомендуемых 200 мкм). Когда в 1970-е годы впервые был обнаружен физиологический ответ на ношение мягких контактных линз [19], «затрясло» всю индустрию контактной коррекции зрения, ей срочно пришлось искать новые материалы, которые пропускали достаточно кислорода к роговице. Стоит ли нам ожидать подобной реакции на это открытие от современной индустрии и исследователей?
Пока же существующие клинические исследования подтверждают существование гипоксического ответа на ношение склеральных линз, который наблюдается в разных слоях роговицы, особенно когда слезный резервуар под линзой имеет увеличенную глубину.
Механизмы компенсации
В качестве потенциальных альтернативных путей транспорта кислорода к роговице можно было бы рассматривать обмен слезы и ее перемешивание при ношении склеральных линз. Однако недавние исследования слезообмена под склеральными линзами показали, что после стабилизации линзы на глазу он минимальный (менее 0,5% в минуту), что существенно ниже этого показателя при ношении мягких контактных линз (примерно 6% в минуту) [20, 21]. Соответственно, нельзя считать слезообмен действенным механизмом, способным устранить гипоксический стресс во время ношения склеральных линз, особенно в тех случаях, когда периферия линзы хорошо подогнана к форме склеры и конъюнктивы под ней, квадрант за квадрантом, что увеличивает вероятность «запечатывания» слезного резервуара.
В отличие от слезообмена, перемешивание слезы понимается как процесс, который происходит при моргании или движениях глаз, во время чего склеральная линза перемещается по конъюнктиве и производит тем самым движение жидкости в резервуаре слезы под ней. Та часть жидкости, которая внизу резервуара, ближе к роговице, в таком случае подниматься вверх, к задней поверхности линзы, где теоретически может обогатиться кислородом из воздуха. Перемешивание слезы под склеральной линзой ограниченно [22], но, если оно есть, его можно усилить, когда линза подобрана с неглубоким резервуаром слезы.
Некоторые склеральные линзы могут быть модернизированы для увеличения обмена слезы; например, их можно изготовить с периферическими кривыми, образующими канальчики [23], или с более свободной посадкой на периферии. Обе стратегии способны усилить слезообмен и доставить к роговице не достаточный для нее объем кислорода, даже несмотря на большую глубину резервуара и толщину самой линзы. Возможно также просверливание отверстий, это снижает гипоксическую нагрузку на роговицу [24]. В тех случаях, когда склеральные линзы просто необходимы в силу того, что состояние роговицы зашло в такую стадию, в которой применение других линз невозможно, специалистам нужно оценить соотношение «польза – риск». Гипоксический стресс, вызванный толстой линзой или глубоким резервуаром под ней, может быть менее значительным фактором, нежели восстановление зрения, купирование болевого синдрома или реабилитация поверхности глаза.
Знаки гипоксии
При отеке роговицы, составляющем примерно 5%, наблюдается снижение ее прозрачности; при 10%-м отеке могут появляться стромальные складки [25]. Поэтому неудивительно, что знаки отека роговицы, вызванного ношением современных склеральных линз на здоровых глазах (он составляет 1–3%), часто не регистрируются при биомикроскопии. Но это не означает, что на субклиническом уровне не существует гипоксического стресса.
Васкуляризация – это локальный ответ в области лимба на гипоксию или механическое раздражение. В случае склеральных линз глубина слезного резервуара над зоной лимба редко превышает 100 мкм, что ведет практически к невозможности появления сколь-либо значительного гипоксического стресса. Поэтому васкуляризацию не наблюдают, разве что в случае скомпрометированных роговиц (после пересадки), пролонгированного ношения линз или касания лимба задней поверхностью линзы. Механическое раздражение, вызванное посадкой линзы на лимб, может привести к нарушению плотных связей клеток эпителия, так что между ними начнется накопление жидкости (что неверно называют буллами) [26]. В свою очередь, такие структурные изменения могут вызвать иммунный ответ, проявляющийся в инвазии кровяных клеток в роговицу.
Учитывая эти аспекты, специалисту нелегко точно количественно оценить и динамически наблюдать гипоксический стресс (субклинический отек) у пациентов, носящих склеральные линзы [27]. В принципе можно применить неконтактную пахиметрию (но она потребует снятия линзы) [28] либо оптическую когерентную томографию, с тем чтобы оценить в процентах отек роговицы в каждом из ее слоев [14]. Еще одна возможная техника – это конфокальная микроскопия [29], но ее в основном используют ученые, и получить к ней доступ рядовому офтальмологу не так просто.
Другие клинические вопросы
Появление в слезном органического мусора может служить потенциальным индикатором гипоксического стресса. Скопление белых органических частиц (затуманивание) способно серьезно ухудшить остроту зрения, так что пользователю придется время от времени снимать линзу днем для того, чтобы сполоснуть ее и наполнить резервуар чистой слезой [3]. Недавно в резервуарах пользователей склеральных линз были обнаружены белые кровяные клетки, обладающие воспалительным потенциалом [30], они предрасполагают глазную поверхность к воспалению [31]. Затуманивание зрения органическим мусором было в 2,24 раза больше на каждые дополнительные 50 мкм увеличения слезного резервуара свыше 200 мкм. Хотя такое затуманивание может быть причиной либо следствием стресса роговицы, накопление органического мусора является многофакторным, на него оказывают влияние также посадка линзы на периферии и характер слезного обмена. Для того чтобы значительно снизить накопление мусора в слезном резервуаре, рекомендуется уменьшать его глубину в центре (делать ее меньше 200 мкм) и в области лимба (меньше 70 мкм).
Уроки, полученные от применения мягких линз
В настоящее время у нас нет проспективных исследований, в которых изучалось бы долговременное ношение склеральных линз. Тем не менее мы можем обратиться к клиническим результатам исследования пациентов, которые длительное время в 80-е годы прошлого века носили линзы с низким показателем пропускания кислорода (Dk/t). Очевидно, что у ряда пациентов роговицы были серьезно изменены в силу хронического гипоксического стресса [32], хотя и размер отека в те годы сильно превышал обсуждаемые в этой статье 1–3% [33]. В некоторых случаях, когда гипоксический стресс затрагивал функции эндотелия, роговичная декомпенсация выглядела словно осложнение катарактальной хирургии [33]. Значит ли это, что у пациентов, которым подобраны современные склеральные линзы и у которых наблюдался незначительный гипоксический стресс, с течением времени будут подвержены повышенному риску осложнений со стороны роговицы? Ответ на этот вопрос еще не получен, поэтому пока специалистам остается лишь следовать принципу «не навреди», тщательно взвешивать все риски, оценивать пользу и целесообразность назначения того или иного типа контактных линз пациенту.
Можем ли мы улучшить ситуацию?
Вне зависимости от состояния пациента, глазной поверхности, выбранного для него дизайна линзы или ее диаметра любая склеральная линза должна подбираться так, чтобы минимизировать гипоксический стресс. А это означает ограничение толщины линзы, выбор материала с высокой кислородной проницаемостью, снижение глубины слезного резервуара, а также уменьшение времени ношения линз для ряда пациентов. В одном исследовании прозвучало, что именно толщина линзы, а не глубина слезного резервуара под ней, служит значимым фактором, ведущим к гипоксическому стрессу [11]. Это противоречит имеющимся у нас теоретическим моделям, построенным на понимании проницаемости жидкостей и растворов [34]. Но если это так, то это указание производителям выпускать более тонкие склеральные линзы.
Возможной проблемой при подборе тонких линз является их повышенная гибкость и возникающий в результате астигматизм. В одном из исследований [35], а также в неопубликованной работе одного из авторов настоящей статьи (Л. Мичо) изучалась гибкость склеральной линзы как функция толщины в центре. Оказалось, что ее можно существенно понизить (вплоть до 150–200 мкм) без значительного влияния на рефракционную картину. Гибкость линзы и возникающий астигматизм выше при использовании тонких, ротационно симметричных линз, надетых на торическую склеру. Однако если в каждом квадранте линза хорошо подогнана к склере (торическая или индивидуальная гаптическая линза), то изгиб поверхности линзы минимален. Стабильность формы линзы может ухудшиться, если она слишком тонкая. Однако снижение ее толщины от 350–400 мкм (типично для многих производителей) до 200–250 мкм может быть разумным в определенном диапазоне значений миопии. Есть необходимые увеличения толщины линзы в силу ее оптической силы (выпуклые линзы) или диаметра (линзы с большим диаметром должны быть слегка толще) – их можно компенсировать выбором материала с высокой кислородной проницаемостью (сейчас есть с показателем даже 200 ед.) либо снижением глубины резервуара.
Все сводится к балансу пользы и рисков
Принимая во внимание все данные контролируемых клинических исследований, практикующие врачи должны стремиться свести к минимуму риск возможной гипоксии роговицы, изменяя, когда это возможно, конструкцию и форму линзы, материал линзы и время ношения. Такой минимизации риска они могут достичь этого с помощью любой склеральной линзы. Потенциальные риски и преимущества ношения склеральной линзы должны учитываться специалистом применительно к каждому пациенту.Что вы можете сделать, чтобы ограничить риски и максимизировать выгоды? Нужно выбирать линзы с улучшенным транспортом кислорода ради снижения любого хронического стресса, связанного с гипоксией – это безусловно, является одним из факторов, который следует учитывать. Мы считаем, что, , если склеральные линзы будут назначаться пациенту в течение многих лет, адаптация подходящих стратегий для облегчения гипоксии, особенно в случаях скомпрометированных роговиц с ослабленным механизмом эндотелиального насоса, является обязательной.
Список литературы
- Nau CB, Harthan J, Shorter E, et al. Demographic Characteristics and Prescribing Patterns of Scleral Lens Fitters: The SCOPE Study. Eye Contact Lens. 2018; 44 Suppl 1: S265–S272.
- van der Worp E, Bornman D, Ferreira DL, Faria-Ribeiro M, Garcia-Porta N, González-Méijome JM. Modern scleral contact lenses: A review. Cont Lens Anterior Eye. 2014 Aug; 37: 240–250.
- Walker MK, Bergmanson JP, Miller WL, Marsack JD, Johnson LA. Complications and fitting challenges associated with scleral contact lenses: A review. Cont Lens Anterior Eye. 2016 Apr; 39: 88–96.
- Hastings GD, Applegate RA, Nguyen LC, Kauffman MJ, Hemmati RT, Marsack JD. Comparison of Wavefront-guided and Best Conventional Scleral Lenses after Habituation in Eyes with Corneal Ectasia. Optom Vis Sci. 2019 Apr; 96: 238–247.
- Fadel D, Kramer E. Potential contraindications to scleral lens wear. Cont Lens Anterior Eye. 2019 Feb; 42: 92–103.
- Michaud L, van der Worp E, Brazeau D, Warde R, Giasson CJ. Predicting estimates of oxygen transmissibility for scleral lenses. Cont Lens Anterior Eye. 2012 Dec; 35: 266–271.
- Compañ V, Aguilella-Arzo M, Edrington TB, Weissman BA. Modeling Corneal Oxygen with Scleral Gas Permeable Lens Wear. Optom Vis Sci. 2016 Nov; 93: 1339–1348.
- Bergmanson JP, Ezekiel DF, van der Worp E. Scleral contact lenses and hypoxia: Theory versus practice. Cont Lens Anterior Eye. 2015 Jun; 38: 145–147.
- Schornack MM. Scleral lenses: a literature review. Eye Contact Lens. 2015 Jan; 41: 3–11.
- He X, Donaldson KE, Perez VL, Sotomayor P. Case Series: Overnight Wear of Scleral Lens for Persistent Epithelial Defects. Optom Vis Sci. 2018 Jan; 95: 70–75.
- Kim YH, Tan B, Lin MC, Radke CJ. Central Corneal Edema with Scleral-Lens Wear. Curr Eye Res. 2018 Nov; 43: 1305–1315.
- Esen F, Toker E. Influence of Apical Clearance on Mini-Scleral Lens Settling, Clinical Performance, and Corneal Thickness Changes. Eye Contact Lens. 2017 Jul; 43: 230–235.
- van der Worp E. A Guide to Scleral Lens Fitting [monograph online]. Forest Grove, OR: Pacific University: Pacific University Libraries at CommonKnowledge 2010.
- Vincent SJ, Alonso-Caneiro D, Collins MJ, et al. Hypoxic Corneal Changes following Eight Hours of Scleral Contact Lens Wear. Optom Vis Sci. 2016 Mar; 93: 293–299.
- Vincent SJ, Alonso-Caneiro D, Collins MJ. The time course and nature of corneal oedema during sealed miniscleral contact lens wear. Cont Lens Anterior Eye. 2019 Feb; 42: 49–54.
- Giasson CJ, Morency J, Melillo M, Michaud L. Oxygen Tension Beneath Scleral Lenses of Different Clearances. Optom Vis Sci. 2017 Apr; 94: 466–475.
- Giasson CJ. Surface Area of Endothelial Blebs and Cells after the Wear of Scleral Lenses of Different Clearances. Optom Vis Sci. 2019; In Press.
- Holden BA, Williams L, Zantos SG. The etiology of transient endothelial changes in the human cornea. Invest Ophthalmol Vis Sci. 1985 Oct; 26: 1354–1359.
- Zantos SG, Holden BA. Transient endothelial changes soon after wearing soft contact lenses. Am J Optom Physiol Opt. 1977 Dec; 54: 856–858.
- Skidmore KV, Walker MK, Marsack JD, Bergmanson JPG, Miller WL. A measure of tear inflow in habitual scleral lens wearers with and without midday fogging. Cont Lens Anterior Eye. 2019 Feb; 42: 36–42.
- Paugh JR, Chen E, Heinrich C, et al. Silicone Hydrogel and Rigid Gas-Permeable Scleral Lens Tear Exchange. Eye Contact Lens. 2018 Mar; 44: 97–101.
- Tse V, Tan B, Kim YH, Zhou Y, Lin MC. Tear dynamics under scleral lenses. Cont Lens Anterior Eye. 2019 Feb; 42: 43–48.
- Rosenthal P, Croteau A. Fluid-ventilated, gas-permeable scleral contact lens is an effective option for managing severe ocular surface disease and many corneal disorders that would otherwise require penetrating keratoplasty. Eye Contact Lens. 2005 May; 31: 130–134.
- Rathi VM, Mandathara PS, Taneja M, Dumpati S, Sangwan VS. Scleral lens for keratoconus: technology update. Clin Ophthalmol. 2015 Oct 28; 9: 2013–2018.
- Efron N. Contact Lens complications. New York: Butterworth-Heinemann 2004.
- Bergmanson JPG. Clinical Ocular Anatomy and Physiology, 16th Texas Eye Research and Technology Center, 2009.
- Carrasquillo KG, Byrnes S. Corneal Edema and Scleral Lenses. Contact Lens Spectrum. 2018 Nov; 33: 34–41.
- Soeters N, Visser ES, Imhof SM, Tahzib NG. Scleral lens influence on corneal curvature and pachymetry in keratoconus patients. Cont Lens Anterior Eye. 2015 Aug; 38: 294–297.
- Alipour F, Soleimanzade M, Latifi G, Aghaie SH, Kasiri M, Dehghani S. Effects of Soft Toric, Rigid Gas-Permeable, and Mini-Scleral Lenses on Corneal Microstructure Using Confocal Microscopy. Eye Contact Lens. 2019 Apr 18. [Epub ahead of print]
- Postnikoff CK, Pucker AD, Laurent J, Huisingh C, McGwin G, Nichols JJ. Identification of Leukocytes Associated With Midday Fogging in the Post-Lens Tear Film of Scleral Contact Lens Wearers. Invest Ophthalmol Vis Sci. 2019 Jan 2; 60: 226–233.
- Tomlins PJ, Nunnick J, Malladi R, Rauz S, Curnow J. Characterisation of the Ocular Surface Leukocyte Populations before and after Haemopoietic Stem Cell Transplant in Patients with and without Ocular Disease. Invest Ophthalmol Vis Sci. 2014 Apr; 55: 4065.
- Holden BA. The Glenn A. Fry Award lecture 1988: the ocular response to contact lens wear. Optom Vis Sci. 1989 Nov; 66: 717–733.
- Sharma N, Singhal D, Nair SP, Sahay P, Sreeshankar SS, Maharana P. Corneal edema after phacoemulsification. Indian J Ophthalmol. 2017 Dec; 65: 1381–1389.
- Benjamin WJ. Oxygen transport through contact lenses. In Guillon M, Ruben M, Eds. Contact Lens Practice. London UK: Chapmann Hall Medical Publishers 1994: 47–69.
- Vincent SJ, Kowalski LP, Alonso-Caneiro D, Kricancic H, Collins MJ. The influence of centre thickness on miniscleral lens flexure. Cont Lens Anterior Eye. 2019 Feb; 42: 63–69.
Авторы: Л. Мичо, оптометрист, профессор, начальника отдела изучения контактных линз Монреальского университета (Монреаль, Канада); С. Винсент, д-р филос., оптометрист, доцент кафедры оптометрии и науки о зрении Квинслендского технологического университета (Квинсленд, Австралия)
Перевод: И. В. Ластовская
Статья опубликована в журнале Contact Lens Spectrum (01.10.2019). Журнал выпускается компанией PentaVision LLC (Амблер, Пенсильвания, США). © PentaVision LLC, 2020. Больше информации см. на сайте компании: www.visioncareprofessional.com. Перевод печатается с разрешения PentaVision LLC
Copyright © РА «Веко»
Печатная версия перевода статьи опубликована в журнале «Современная оптометрия» [2020. № 2 (132)].
По вопросам приобретения журналов и оформления подписки обращайтесь в отдел продаж РА «Веко»:
- Тел.: (812) 603-40-02.
- E-mail: magazine@veko.ru
- veko.ru
Наши страницы в соцсетях: