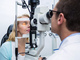
В статье говорится о способах исследования боли на поверхности глаза и ее лечении.
- Болевые ощущения со стороны поверхности глаза и их происхождение
- Что нам известно: диагностика
- Что нам известно: лечение
- В каком направлении мы движемся?
- Заключение
Болевые ощущения со стороны поверхности глаза и их происхождение
Международная ассоциация по изучению боли (International Association for the Study of Pain – IASP) определяет это понятие как «неприятное сенсорное и/или эмоциональное переживание, связанное с фактическим или потенциальным повреждением тканей или напоминающее о нем» [1]. Поскольку глаз является органом, который мы обычно не чувствуем, такое определение может быть распространено на боль, возникающую на его поверхности, она часто описывается пациентами как ощущение сухости, жжения, рези, раздражения и/или болезненности. Эта боль – одна из основных причин инвалидности, заболеваемости, из-за нее ухудшается качество жизни. Интерес к ее изучению в последнее время усилился в связи с тем, что она коррелирует с растущим количеством посещений глазных клиник и затратами на офтальмологическое лечение во всем мире [2]. Боль на поверхности глаза может быть вызвана ноцицептивными, невропатическими или смешанными механизмами.
Ноцицептивная боль образуется в результате фактического или угрожающего повреждения ненервной ткани и обусловлена активацией ноцицепторов [1]. Получается, она возникает из-за стимулов, которые непосредственно активируют ноцицепторы на поверхности органа зрения. Ноцицептивная боль может быть преходящей, как в случае с абразией роговицы, или хронической из-за различных причин, включая патологию слезной пленки (например, снижение слезоотделения, повышенная осмолярность слезы, воспаление), факторы окружающей среды (загрязнение воздуха и климат), аномальную анатомию, прямое повреждение тканей глаза или хирургическое вмешательство [3].
Невропатическая боль вызвана поражением или заболеванием соматосенсорной нервной системы [1]. Если применить это определение к поверхности глаза, невропатическая боль является результатом патологических изменений в тройничном нерве, который иннервирует роговицу и ткани орбиты (периферическая невропатическая боль) или в нейронах более высокого уровня, соединяющих поверхность глаза с мозгом (центральная невропатическая боль). Поскольку постоянные (например, при хроническом сухом глазе) или серьезные (такие как хирургическое повреждение нерва) ноцицептивные источники боли могут приводить к нарушениям периферических и центральных нервов, неудивительно, что боль на поверхности глаза часто имеет смешанную этиологию, образованную как ноцицептивными, так и невропатическими факторами [3].
Что нам известно: диагностика
Хотя о нейропатической боли мы знаем гораздо меньше по сравнению с ноцицептивной глазной болью, растущий интерес к этой теме позволил выработать приблизительную основу для диагностики и лечения пациентов с невропатическими болевыми симптомами. Важно подчеркнуть, что наша текущая база знаний и диагностические возможности ограничены, поэтому крайне важно провести дальнейшие исследования нейропатической боли, возникающей на поверхности глаза. Это позволит более полно понять ее происхождение и предоставит эффективные инструменты для диагностики, которые обеспечат индивидуальный менеджмент пациента. Текущие трудности включают в себя клинические показатели, которые непоследовательно оцениваются у всех пациентов, ограниченное количество клинических тестов, доступных для изучения функции роговичного нерва, и отсутствие «золотого стандарта» определения для возникающей на поверхности глаза невропатической боли.
В связи с этим во время приема пациентов необходимо сосредоточиться на проведении тщательной оценки состояния поверхности органа зрения для изучения потенциальных ноцицептивных источников боли. Кроме того, нужно искать свидетельства тому, какие нейропатические механизмы способствуют возникновению боли. Первым шагом является получение подробного анамнеза, в котором содержится информация о сопутствующих глазных и системных заболеваниях и принимаемых человеком лекарствах. Это полезно, поскольку специфические системные состояния ассоциированы с характерными проявлениями на поверхности глаза. Например, ревматоидный артрит более тесно связан с недостатком слезной жидкости и воспалением глазной поверхности, а мигрень – с нейропатической болью на поверхности органа зрения [4]. Апноэ во сне (и сопутствующее лечение с помощью создания постоянного положительного давления в дыхательных путях), с другой стороны, возникает из-за анатомических аномалий (например, дряблости век) и повреждений поверхности глаза.
Затем следует использовать стандартизированные опросники для количественной оценки и характеристики глазной боли. Это могут быть специальные опросники, например «Опросник по поводу сухого глаза» (Dry Eye Questionnaire 5 – DEQ5), в котором задаются вопросы о частоте и интенсивности сухости и дискомфорта, а также о слезной жидкости [5], или «Индекс заболеваний глазной поверхности» (Ocular Surface Disease Index – OSDI) – многоаспектный опросник, включающий в себя вопросы о частоте различных дескрипторов, влиянии триггеров и воздействии болезни на качество жизни [6]. Можно также применять опросники, касающиеся боли на поверхности глаза, такие как числовая шкала оценки (numerical rating scale – NRS) типа Лайкерта, «Опросник оценки глазной боли» (Ocular Pain Assessment Survey – OPAS), в котором спрашивается об интенсивности боли, дескрипторах и о влиянии на качество жизни [7], или «Перечень симптомов невропатической боли, модифицированный для глаз» (Neuropathic Pain Symptom Inventory-modified for the Eye – NPSI-E); благодаря его использованию можно выяснить интенсивность дескрипторов невропатической боли [8].
Осмотр начинается с изучения кожи вокруг глаз, частоты моргания и анатомических особенностей. Далее могут быть применены тесты для оценки степени воспаления глазной поверхности или осмолярности слезы, то есть распространенных источников ноцицептивной боли. Затем чувствительность роговицы можно качественно протестировать с помощью аппликатора с ватным наконечником или зубной нити и оценить ее по шкале от 0 до 3, где 0 обозначает отсутствие чувствительности, 1 – ее снижение, 2 – нормальную чувствительность и 3 – повышенную. Следует провести обследование с помощью щелевой лампы с окрашиванием красителем для оценки края века (на предмет переднего блефарита и/или признаков дисфункции мейбомиевых желез), стабильности слезной пленки (со временем разрыва слезы), окрашивания роговицы и конъюнктивы, а также анатомии конъюнктивы. Слезоотделение можно оценить благодаря применению теста Ширмера, хотя высота слезного мениска часто используется в качестве альтернативной меры. Врачу важно осмотреть пациента перед введением анестетика, поскольку это может повлиять на результаты обследования с помощью щелевой лампы; введение анестетика само по себе является важным клиническим испытанием. Если присутствует боль на глазной поверхности, врач должен сначала попросить пациента оценить ее интенсивность по шкале 0–10 NRS, затем закапать капли анестетика, а после, через 0,5–2 мин, повторно оценить боль. Постоянная боль после местной анестезии предполагает наличие центрального или неокулярного поверхностного источника боли. Наконец, для изучения морфологии роговичного нерва могут быть проведены тесты визуализации, такие как конфокальная микроскопия in vivo.
Ключевые факторы, которые свидетельствуют о потенциальном возникновении невропатической боли на поверхности глаза, хотя и не со 100 %-й вероятностью:
1. Наличие у пациента сопутствующих хронических болей в анамнезе (например, фибромиалгия, мигрень, сложный регионарный болевой синдром, хроническая тазовая боль, вульводиния).
2. Наличие определенных ответов в опросниках (например, жгучая боль, чувствительность к ветру или свету или симптомы, несоразмерные признакам заболевания).
3. Аномальная чувствительность роговицы (гипо- или гиперестезия) [9].
4. Стойкие симптомы, несмотря на многократную терапию ноцицептивной боли в анамнезе [3, 10–12].
Как подчеркивалось ранее, некоторые результаты могут говорить о локализации аномалии. В частности, постоянная боль после закапывания местного анестетика, а также признаки кожной аллодинии (боль при легком прикосновении вокруг глаза) указывают на центральную (например, связанную с центральной нервной системой) аномалию [13].
Что нам известно: лечение
Поскольку диагноз невропатической боли является клиническим, первый шаг в ее устранении – лечение всех ноцицептивных источников боли. Если эта стратегия не увенчалась успехом или если первичное обследование точно указывает на невропатическую боль, следует начать ее лечение.
Терапия первой линии у пациентов с периферической невропатической болью местная. Она включает в себя лечение противовоспалительными средствами и препаратами на основе крови, например аутологичной сывороточной слезой (АСС) или обогащенной тромбоцитами плазмой. В различных сериях статей было показано, что противовоспалительная терапия купирует болевые симптомы [14], устраняет аномалии поверхности слезы [15] и улучшает показатели периферических нервов, такие как плотность нервов роговицы [16] у группы людей. Препараты на основе крови для местного применения содержат связанные с кровью нейротрофические и эпителиальные факторы роста, включая фактор роста нервов (ФРН) и нейротрофин-3, которые могут способствовать регенерации нервов роговицы [17]. Несколько исследований показали купирование болей [18] и улучшение показателей периферических нервов [19] с помощью АСС. В настоящее время в доклинических исследованиях изучается использование модуляторов переходного потенциала рецепторов катионных каналов подсемейства V члена 1 (TrpV1) для лечения периферической невропатической боли после хирургических вмешательств [20, 21] и химиотерапии [22, 23]. Эта терапия также изучается в исследованиях с участием пациентов с послеоперационной хронической болью в роговице (См. исследование NCT04630158 на сайте: clinicaltrials.gov).
Терапия первой линии у пациентов с центральной невропатической болью включает в себя назначение пероральных нейромодуляторов, таких как α2δ лиганды (габапентин или прегабалин), трициклические антидепрессанты (нортриптилин или амитриптилин), ингибиторы обратного захвата серотонина и норадреналина (дулоксетин) и противосудорожные средства, блокирующие натриевые каналы (карбамазепин или топирамат) [24, 25]. Поскольку эти средства являются нейромодуляторами, а не прямыми анальгетиками, купирование боли впервые наблюдается примерно через 3 месяца после достижения терапевтической дозы и продолжается постепенно с течением времени. Таким образом, пациенты должны быть подробно проинформированы об ожиданиях, преимуществах, рисках и продолжительности курса лечения для обеспечения соблюдения режима терапии.
В каком направлении мы движемся?
В связи с отсутствием определения «золотого стандарта» диагностики и возможности выявить локализацию нервной дисфункции невропатическая боль таит в себе много загадок, которые еще предстоит разгадать. Необходимы дальнейшие исследования для улучшения диагностики и менеджмента терапии. К счастью, новые методы лечения, изучаемые как в клинических, так и в доклинических исследованиях, на данный момент демонстрируют многообещающие результаты.
Другие методы лечения периферической боли у людей, исследуемые в настоящее время, включают в себя трансплантацию амниотической мембраны (ТАМ) [26] и рекомбинантный человеческий ФРН [27]. На ранней стадии в открытом пилотном исследовании в Корее 15 пациентам с нейропатической болью, ассоциированной с болезнью сухого глаза, применяли агонист TRPM8 cryosim-3 четыре раза в день. Судя по «Опроснику оценки глазной боли», боль (шкала 0–60) уменьшилась через 1 неделю (26,47 ± 11,45; р = 0,01) и 1 месяц (21,53 ± 10,84; р = 0,02) по сравнению с исходным уровнем (30,60 ± 12,84), в то время как качество жизни (шкала 0–60) улучшилось аналогичным образом (1 неделя: 27,60 ± 15,49, 1 месяц: 27,17 ± 16,06, исходное значение: 33,53 ± 14,24; р = 0,003 и 0,02 соответственно) [28]. Между тем местные препараты агентов, связывающих TRP (агонисты, антагонисты и модуляторы, такие как резинифератоксин) [29, 30], производные омега-3 жирных кислот (например, докозаноиды) [31, 32] и терапия агонистами каннабиноидов изучаются на доклинических стадиях [33, 34].
В настоящее время исследуется несколько новых методов лечения централизованной боли. К ним относятся пероральные препараты (низкие дозы налтрексона или трамадола) [35, 36] и адъювантная терапия, нацеленная на периокулярные афференты. Например, блокаторы периокулярного нерва (обратимый блокатор натриевых каналов в сочетании с кортикостероидом длительного действия) использовались у людей с кожной аллодинией [37]. Учитывая связь между мигренью и нейропатической болью в глазной поверхности, стратегии, используемые при мигрени, также были изучены для лечения боли в глазной поверхности. К ним относятся инъекции ботулинического токсина (ингибирует высвобождение нейровозбуждающих передатчиков) [38–40] и неинвазивные устройства для нейростимуляции, такие как чрескожная электрическая стимуляция нервов и транскраниальная магнитная стимуляция [41–43]. Принимая во внимание тесную связь между хронической болью в глазной поверхности и психологической дисфункцией [44], важно учитывать эмоциональный компонент; этого можно достичь с помощью когнитивно-поведенческой терапии наряду с другими методами лечения [45]. Необходимы дальнейшие исследования, чтобы определить, когда вегетативные механизмы способствуют хронической боли в глазной поверхности; однако в отдельных случаях использовались стратегии воздействия на эти механизмы путем блокирования клиновидно-небного (парасимпатического) или верхнего шейного (симпатического) ганглия. В целом, остающейся проблемой является необходимость точной медицины, поскольку в настоящее время невозможно предсказать, какой пациент лучше всего отреагирует на какую-либо конкретную терапию, будь то изолированная или комбинированная.
Заключение
По мере того как мы сталкиваемся с ростом числа обращений пациентов и преодолеваем разрыв с нашим нынешним пониманием ее аналога – ноцицептивной болью, наши знания о нейропатической боли на поверхности глаза постоянно растут. Несмотря на то что это развивающаяся область, недавно была создана основа для клинической диагностики и начала терапии невропатической боли на глазной поверхности. Достижения как в сфере диагностических технологий, так и в терапевтических алгоритмах остаются основными целями для совершенствования в этой области. Кроме того, важно найти больше терапевтических способов, поскольку они укрепят профилактические и лечебные методы улучшения часто очень резистентных симптомов. На данный момент для достижения оптимальных результатов необходимы подход, ориентированный на пациента, и использование мультимодальных методов лечения, которые применяются в течение длительного периода времени при надлежащем консультировании пациента.
Список литературы
1. IASP Terminology: International Association for the Study of Pain; 2020 [Available from: https://www.iasp-pain.org/Education/Content.aspx?ItemNumber=1698.].
2. Mertzanis P, Abetz L, Rajagopalan K, et al. The relative burden of dry eye in patients’ lives: comparisons to a U.S. normative sample. Invest Ophthalmol Vis Sci. 2005 Jan; 46 (1): 46–50.
3. Mehra D, Cohen NK, Galor A. Ocular Surface Pain: A Narrative Review. Ophthalmol Ther. 2020; 9 (3): 1–21.
4. Lee Y, Kim M, Galor A. Beyond dry eye: how co-morbidities influence disease phenotype in dry eye disease. Clin Exp Optom. 2022; 105 (2): 177–185.
5. Chalmers RL, Begley CG, Caffery B. Validation of the 5-Item Dry Eye Questionnaire (DEQ-5): Discrimination across self-assessed severity and aqueous tear deficient dry eye diagnoses. Cont Lens Anterior Eye. 2010; 33 (2): 55–60.
6. Schiffman RM, Christianson MD, Jacobsen G, et al. Reliability and validity of the Ocular Surface Disease Index. Arch Ophthalmol. 2000; 118 (5): 615–21.
7. Qazi Y, Hurwitz S, Khan S, et al. Validity and Reliability of a Novel Ocular Pain Assessment Survey (OPAS) in Quantifying and Monitoring Corneal and Ocular Surface Pain. Ophthalmology. 2016; 123 (7): 1458–68.
8. Farhangi M, Feuer W, Galor A, et al. Modification of the Neuropathic Pain Symptom Inventory for use in eye pain (NPSI-Eye). Pain. 2019; 160 (7): 1541–1550.
9. Galor A, Felix ER, Feuer W, et al. Corneal Nerve Pathway Function in Individuals with Dry Eye Symptoms. Ophthalmology. 2021; 128 (4): 619–621.
10. Ong ES, Felix ER, Levitt RC, et al. Epidemiology of discordance between symptoms and signs of dry eye. Br J Ophthalmol. 2018; 102 (5): 674–679.
11. Kalangara JP, Galor A, Levitt RC, et al. Characteristics of Ocular Pain Complaints in Patients With Idiopathic Dry Eye Symptoms. Eye Contact Lens. 2017; 43 (3): 192–198.
12. Galor A, Batawi H, Felix ER, et al. Incomplete response to artificial tears is associated with features of neuropathic ocular pain. Br J Ophthalmol. 2016; 100 (6): 745–9.
13. Crane AM, Feuer W, Felix ER, et al. Evidence of central sensitisation in those with dry eye symptoms and neuropathic-like ocular pain complaints: incomplete response to topical anaesthesia and generalised heightened sensitivity to evoked pain. Br J Ophthalmol. 2017; 101 (9): 1238–1243.
14. Devecı H, Kobak S. The efficacy of topical 0.05 % cyclosporine A in patients with dry eye disease associated with Sjögren’s syndrome. Int Ophthalmol. 2014; 34 (5): 1043–8.
15. Sall K, Stevenson OD, Mundorf TK, Reis BL. Two multicenter, randomized studies of the efficacy and safety of cyclosporine ophthalmic emulsion in moderate to severe dry eye disease. CsA Phase 3 Study Group. Ophthalmology. 2000; 107 (4): 631–9.
16. Levy O, Labbé A, Borderie V, et al. Increased corneal sub-basal nerve density in patients with Sjögren syndrome treated with topical cyclosporine A. Clin Exp Ophthalmol. 2017; 45 (5): 455–463.
17. Aggarwal S, Colon C, Kheirkhah A, Hamrah P. Efficacy of autologous serum tears for treatment of neuropathic corneal pain. Ocul Surf. 2019; 17 (3): 532–539.
18. Ali TK, Gibbons A, Cartes C, et al. Use of Autologous Serum Tears for the Treatment of Ocular Surface Disease From Patients With Systemic Autoimmune Diseases. Am J Ophthalmol. 2018; 189: 65–70.
19. Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. Autologous Serum Tears for Treatment of Photoallodynia in Patients with Corneal Neuropathy: Efficacy and Evaluation with In Vivo Confocal Microscopy. Ocul Surf. 2015; 13 (3): 250–62.
20. Huang YK, Lu YG, Zhao X, et al. Cytokine activin C ameliorates chronic neuropathic pain in peripheral nerve injury rodents by modulating the TRPV1 channel. Br J Pharmacol. 2020; 177 (24): 5642–5657.
21. Kim HY, Park CK, Cho IH, et al. Differential Changes in TRPV1 expression after trigeminal sensory nerve injury. J Pain. 2008; 9 (3): 280–8.
22. Ba X, Wang J, Zhou S, et al. Cinobufacini protects against paclitaxel-induced peripheral neuropathic pain and suppresses TRPV1 up-regulation and spinal astrocyte activation in rats. Biomed Pharmacother. 2018; 108: 76–84.
23. Hao Y, Luo X, Ba X, et al. Huachansu suppresses TRPV1 up-regulation and spinal astrocyte activation to prevent oxaliplatin-induced peripheral neuropathic pain in rats. Gene. 2019; 680: 43–50.
24. Patel S, Hwang J, Mehra D, Galor A. Corneal Nerve Abnormalities in Ocular and Systemic Diseases. Exp Eye Res. 2021; 202: 108284.
25. Patel S, Mittal R, Felix ER, et al. Differential Effects of Treatment Strategies in Individuals With Chronic Ocular Surface Pain With a Neuropathic Component. Front Pharmacol. 2021; 12: 788524.
26. Morkin MI, Hamrah P. Efficacy of self-retained cryopreserved amniotic membrane for treatment of neuropathic corneal pain. Ocul Surf. 2018; 16 (1): 132–138.
27. Sacchetti M, Lambiase A, Schmidl D, et al. Effect of recombinant human nerve growth factor eye drops in patients with dry eye: a phase IIa, open label, multiple-dose study. Br J Ophthalmol. 2020; 104 (1): 127–135.
28. Yoon HJ, Kim J, Yang JM, et al. Topical TRPM8 Agonist for Relieving Neuropathic Ocular Pain in Patients with Dry Eye: A Pilot Study. J Clin Med. 2021; 10 (2): 250.
29. Venkatachalam K, Montell C. TRP channels. Annu Rev Biochem. 2007; 76: 387–417.
30. Yang JM, Wei ET, Kim SJ, Yoon KC. TRPM8 Channels and Dry Eye. Pharmaceuticals (Basel). 2018; 11 (4): 125.
31. Rashid S, Jin Y, Ecoiffier T, et al. Topical omega-3 and omega-6 fatty acids for treatment of dry eye. Arch Ophthalmol. 2008; 126 (2): 219–25.
32. Pham TL, Bazan HEP. Docosanoid signaling modulates corneal nerve regeneration: effect on tear secretion, wound healing, and neuropathic pain. J Lipid Res. 2021; 62: 100033.
33. Thapa D, Cairns EA, Szczesniak AM, et al. Allosteric Cannabinoid Receptor 1 (CB1) Ligands Reduce Ocular Pain and Inflammation. Molecules. 2020; 25 (2): 417.
34. Thapa D, Cairns EA, Szczesniak AM, et al. The Cannabinoids Δ8THC, CBD, and HU-308 Act via Distinct Receptors to Reduce Corneal Pain and Inflammation. Cannabis Cannabinoid Res. 2018; 3 (1): 11–20.
35. Jackson D, Singh S, Zhang-James Y, Faraone S, Johnson B. The Effects of Low Dose Naltrexone on Opioid Induced Hyperalgesia and Fibromyalgia. Front Psychiatry. 2021; 12: 593842.
36. Hutchinson MR, Zhang Y, Brown K, et al. Non-stereoselective reversal of neuropathic pain by naloxone and naltrexone: involvement of toll-like receptor 4 (TLR4). Eur J Neurosci. 2008; 28 (1): 20–9.
37. Small LR, Galor A, Felix ER, et al. Oral Gabapentinoids and Nerve Blocks for the Treatment of Chronic Ocular Pain. Eye Contact Lens. 2020; 46 (3): 174–181.
38. Diel RJ, Kroeger ZA, Levitt RC, et al. Botulinum Toxin A for the Treatment of Photophobia and Dry Eye. Ophthalmology. 2018; 125 (1): 139–140.
39. Diel RJ, Hwang J, Kroeger ZA, et al. Photophobia and sensations of dryness in patients with migraine occur independent of baseline tear volume and improve following botulinum toxin A injections. Br J Ophthalmol. 2019; 103 (8): 1024–1029.
40. Venkateswaran N, Hwang J, Rong AJ, et al. Periorbital botulinum toxin A improves photophobia and sensations of dryness in patients without migraine: Case series of four patients. Am J Ophthalmol Case Rep. 2020; 19: 100809.
41. Johnson M. Transcutaneous Electrical Nerve Stimulation: Mechanisms, Clinical Application and Evidence. Rev Pain. 2007; 1 (1): 7–11.
42. Dieckmann G, Fregni F, Hamrah P. Neurostimulation in dry eye disease-past, present, and future. Ocul Surf. 2019; 17 (1): 20–7.
43. Mehra D, Mangwani-Mordani S, Acuna K, et al. Long-Term Trigeminal Nerve Stimulation as a Treatment for Ocular Pain. Neuromodulation. 2021; 24 (6): 1107–1114.
44. Patel S, Felix ER, Levitt RC, et al. Dysfunctional Coping Mechanisms Contribute to Dry Eye Symptoms. J Clin Med. 2019; 8 (6): 901.
45. Otis JD, Sanderson K, Hardway C, et al. A randomized controlled pilot study of a cognitive-behavioral therapy approach for painful diabetic peripheral neuropathy. J Pain. 2013; 14 (5): 475–82.
Авторы:
А. Галор, врач-офтальмолог, специалист по роговице и увеиту с двойным назначением в Медицинском центре по делам ветеранов Майами (Вирджиния) и Глазном институте Бэскома Палмера, Медицинская школа Миллера Университета Майами (Флорида, США)
С. Патель, врач-офтальмолог, выпускник Медицинской школы Миллера Университета Майами (Флорида, США)
© РА «Веко»
Печатная версия статьи опубликована в журнале «Современная оптометрия» [2022. № 7 (156)].
По вопросам приобретения журналов и оформления подписки обращайтесь в отдел продаж РА «Веко»:
- Тел.: (812) 634-43-34.
- E-mail: magazine@veko.ru
- veko.ru
Наши страницы в соцсетях: