В этой работе опубликованы результаты исследования протеома слезы молодых пациентов, носящих очки, ортокератологические (ОК) линзы и мягкие контактные линзы (МКЛ), с помощью технологии последовательной фрагментации с параллельным накоплением (diaPASEF), не зависящей от данных, и идентифицировано 3406 белковых групп в слезных полосках Ширмера. Наблюдались значительные изменения содержания белка в 19 группах у пользователей ОК-линз и МКЛ. Более того, содержание 82 белковых групп существенно отличалось у детей и молодых людей, носящих очки. В качестве пилотного исследования эта работа обеспечивает глубокий охват протеома слезы и предполагает необходимость изучения реакции глаз на ношение контактных линз (КЛ) у детей и молодых людей по отдельности.
Введение
Жесткие ОК-линзы и МКЛ использовались для замедления прогрессирования миопии, и их применение продолжает расширяться по мере роста эпидемии близорукости [1–4] (Обширный список литературы к статье см. здесь: https://www.sciencedirect.com/science/article/pii/S1874391922002627). Распространенность миопии у взрослых увеличилась с 20–30 % в середине XX века до > 80 % в некоторых частях мира сегодня [5]. Несмотря на пользу для замедления прогрессирования миопии, ношение КЛ является наиболее распространенным триггером воспаления поверхности глаза и может приводить к дискомфорту, боли и даже рубцеванию [6, 7]. Исследования показали, что воспалительные явления роговицы, связанные с ношением КЛ, чаще возникали у подростков и молодых людей в возрасте от 15 до 25 лет [8–11]. Более того, осложнения на поверхности глаза, такие как инфекция конъюнктивы и кератит, возникают у 70 % бессимптомных пользователей КЛ [12]. На сегодняшний день влияние ношения таких линз на поверхность глаза на молекулярном уровне до конца не изучено. В этом исследовании мы рассмотрели протеомы слезы молодых пациентов, носящих ОК-линзы, МКЛ и очки, используя протеомные технологии, базирующиеся на масс-спектрометрии, в частности независимый сбор данных (DIA) в сочетании с параллельным накоплением – серийной фрагментацией (PASEF) в режиме сканирования (diaPASEF).
«Омики», основанные на масс-спектрометрии, оказались привлекательным инструментом для понимания физиологии и патологий биологических систем [13, 14]. Различные технологии масс-спектрометрии – масс-спектрометрия с лазерной десорбцией и ионизацией при помощи матрицы, нативная масс-спектрометрия и восходящая протеомика – использовались для потенциальной идентификации биомаркеров глазных заболеваний, таких как сухость глаз, дисфункция мейбомиевых желез (ДМЖ) и глазные инфекции [15–31]. Однако применение масс-спектрометрии в научных исследованиях, направленных на обнаружение биомаркеров и патологии заболеваний, было ограничено из-за ее чувствительности.
Панорамная протеомика добилась значительных успехов благодаря улучшенной чувствительности, разрешению и скорости масс-спектрометров последних поколений [32–35]. Недавно привлекла значительное внимание технология подвижности захваченных ионов, особенно PASEF в режиме сканирования, она имеет высокую скорость, эффективность и чувствительность [36–38]. В дополнение к другому способу измерения разделения подвижных ионов с высокой скоростью PASEF позволяет анализировать одну их совокупность, одновременно собирая другую. Таким образом, параллельно накапливая и анализируя ионы, с помощью PASEF можно достигнуть рабочего цикла в 100 % без потери чувствительности [36, 37]. При изготовлении масс-спектрометра timsTOF Pro используется технология PASEF, он обеспечивает высокую скорость сканирования – 100 Гц и рабочий цикл примерно в 100 % за счет соединения с квадрупольным анализатором частиц по времени пролета. Такая высокая скорость сканирования дает значительное преимущество в сборе измерений, зависящем от данных (DDA), поскольку с помощью DDA можно отбирать больше молекул-предшественников, тем самым обеспечивая более высокую идентификацию пептидов. Кроме того, timsTOF Pro, основанный на системе высокого разрешения QTOF [39], отличается улучшенными эффективностью пропускания ионов, разрешающей способностью масс-анализаторов и чувствительностью масс-спектрометрического детектора, чтобы удовлетворить потребность в высокой чувствительности. Благодаря этим уникальным преимуществам timsTOF Pro хорошо подходит для протеомного анализа.
Поскольку DDA предназначен для отбора высокоинтенсивных ионов, DIA фрагментирует все ионы в заданной выборке. Это дает более полные данные и высокую воспроизводимость, благодаря чему DDA хорошо подходит для клинических исследований с большими размерами выборки (по количеству субъектов), а также с малым количеством образцов [40–42]. Объединив преимущества PASEF и DIA, diaPASEF демонстрирует свою способность к глубокому охвату протеома и высокую производительность [43, 44].
В данном исследовании мы использовали diaPASEF для профилирования протеомов слезы молодых пациентов, носящих очки, OK-линзы и МКЛ, а также идентифицировали несколько иммунных/воспалительных и метаболических белков, связанных с возрастом и ношением КЛ.
Материал и методы
Дизайн исследования и сбор образцов
Это исследование проводилось в соответствии с принципами Хельсинкской декларации и одобрено комиссией по биомедицинской этике Хьюстонского университета. Перед участием от пациентов было получено письменное согласие. Поскольку среди них находились несовершеннолетние, помимо их согласия, мы также получили разрешение родителей/опекунов.
Молодые люди, регулярно пользующиеся очками и КЛ (более 3 лет ношения), отбирались для участия, если они были в возрасте от 10 до 26 лет, имели наилучшую корригированную остроту зрения 0,8 или выше на каждом глазу, аномалии рефракции от –0,25 до –5,75 дптр при астигматизме менее 1,75 дптр. Было установлено, что участники, носящие КЛ, пользовались ОК-линзами или МКЛ в течение полного рабочего дня (согласно самоотчетам, более четырех дней в неделю в течение как минимум 3 лет). У них не наблюдалось значительного прокрашивания роговицы или конъюнктивы и ДМЖ (≤ степени 1), покраснения поверхности глаза, шероховатости век и покраснения (< степени 2) по шкале Исследовательского центра роговицы и контактных линз (Cornea and Contact Lens Research Unit – CCLRU) [45]. Другими критериями исключения на момент исследования были следующие: активная глазная инфекция или глазные воспалительные заболевания, такие как глазная аллергия или сухость глаз; перенесенная рефракционная/офтальмологическая операция или глазная травма; текущее использование глазных капель, кроме препаратов искусственной слезы; текущее или предыдущее использование аккутана (изоретиноина); беременность или кормление грудью.
Все посещения врача в рамках исследования проходили с 9 до 18 ч с июня 2019 года по февраль 2020-го. Для оценки состояния здоровья глаз проводился осмотр с использованием щелевой лампы по шкале CCLRU [45]. Слезная секреция измерялась на левом глазу с помощью полоски Ширмера (TearFlo, HUB Pharmaceuticals, Скоттсдейл, штат Аризона). Полоску брали руками в перчатках и вынимали через 5 мин или тогда, когда она полностью намокала. Затем эту полоску помещали в чистую пробирку Эппендорфа для забора слезы. В течение часа после сбора ее переносили во льду в морозильную камеру с температурой –80 °C и хранили до анализа партии.
Материалы
Бутилированная вода класса LC-MS (пригодная для жидкостной хроматографии с масс-спектрометрией – ЖХМС), ацетонитрил (ACN), муравьиная кислота (FA) и трипсин для секвенирования были приобретены у Thermo Fisher Scientific (Питтсбург, штат Пенсильвания, США); пептиды iRT – у Biognosys AG (Швейцария). Все остальные химические вещества закупались у компании Millipore Sigma (Сент-Луис) и использовались без дополнительной очистки, если не указано иное.
Подготовка образцов
Каждый образец полоски Ширмера разрезали на куски с помощью стерильного лезвия и погружали в 100 мкл раствора бикарбоната аммония (100 мМ) в пробирке объемом 1,5 мл. Реакции восстановления и алкилирования проводили путем добавления соответственно дитиотреитола (5 мМ) при 37 °C в течение 1 ч и йодоацетамида (10 мМ) на протяжении 30 мин в темноте. Затем добавляли трипсин (1:40 вес/вес) и инкубировали при 37 °C в течение ночи. Реакцию останавливали, добавляя трифторуксусную кислоту. После центрифугирования расщепленные пептиды очищали с использованием хроматографических наконечников C18 Ziptip и высушивали в вакууме с помощью CentriVap (Labconco). Каждый высушенный образец ресуспендировали в 2 %-м ацетонитриле с 0,1 %-й муравьиной кислотой для ЖХМС.
Жидкостная хроматография с масс-спектрометрией
Жидкостная хроматография проводилась на масс-спектрометре timsTOF Pro (Bruker Daltonics, Германия), подключенном к источнику ионов CaptiveSpray. Образцы пептидов (~200 нг) наносили на собственную набивную колонку ReproSil-Pur C18 1,9 мкм (Dr. Maisch GmbH, Германия), 75 мкм × 25 см, температура колонки 40 °C) с буфером A (0,1 %-я муравьиная кислота в воде) и буфером B (0,1 %-я муравьиная кислота в ацетонитриле) в качестве подвижных фаз. 120-минутный градиент составлял 60 мин с буфером В 2–17 %, 90 мин с B до 25 %, 100 мин c B до 37 %, 110 мин с B до 80 % и поддерживался еще 10 мин. Использовалась технология diaPASEF с отношением массы к заряду 64 m/z и заданной выборке подвижных ионов. Напряжение электрораспыления составляло 1,4 кВ, а температура ионообменной трубки – +180 °C. Полные сканы были получены в диапазоне 150–1700 m/z. Энергия столкновения линейно изменялась в зависимости от подвижности: от 27 эВ при 1/K0 = 0,85 см2/(В · с) до 45 эВ при 1/K0 = 1,3 см2/(В · с).
Биоинформатика и статистический анализ
Идентификация и количественный анализ пептидов и белков
Для идентификации и количественного определения пептидов и белков использовалось программное обеспечение (ПО) Spectronaut версии 15 (Biosynosis, Швейцария) с настройками по умолчанию [46]. Коротко говоря, стратегия допуска по динамической массе применялась для извлечения как MS1, так и MS2, и поправочный коэффициент не использовался. Калибровка пептидов iRT выполнялась с помощью метода локальной (нелинейной) регрессии. Для создания ловушек использовался метод мутировавших ловушек. Была включена коррекция интерференции, чтобы при всех прогонах исключить из количественного определения фрагментные ионы с интерференцией. Использовалась собственная библиотека спектров биологических образцов человека. Ее создали с помощью применения модифицированной процедуры, описанной в исследовании Цинь (Qin) и соавторов [47]. Если вкратце, для этой цели было проведено 32 сканирования DDA с разделенными клетками эпителия роговицы и образцами слезы человека, фракционированными с высоким pH. Данные обрабатывались с использованием программного поискового механизма Spectronaut’s Pulsar с настройками по умолчанию. Применялась база UniProt-SwissProt Home Sapiens (Taxon ID 9606, загружена 30.01.2021, 42383 записи). В качестве фиксированной модификации было выбрано карбамидометилирование цистеина, а в качестве переменных модификаций – окисление и ацетилирование метионина. Длина пептида была установлена в диапазоне 7–52, допускались два пропущенных расщепления. Прекурсоры с количеством фрагментов меньше трех были исключены из библиотеки спектров. Частота ложноположительных результатов (ЧЛР) контролировалась на уровне < 1 % при совпадении спектра пептидов, их уровней и белков. Для обработки данных diaPASEF ЧЛР контролировалась на уровне < 1% как для пептидов, так и для белков. Чтобы определить количество представляющих интерес белков, применялась программа Skyline [48] (версия 22.1.9.208). Длина пептида была установлена в диапазоне 6–50. Массы ионов-предшественников и ионов-продуктов были установлены моноизотопными; заряды ионов-предшественников – 2–6, а заряды ионов y- и b-типов – 1–4. Допуск совпадения ионов составлял 0,05 m/z. Минимальное и максимальное значения m/z составили 100 и 1800 соответственно. Остальные параметры были такими же, как указано выше. Необработанные результаты масс-спектрометрии и поиска были переданы в консорциум ProteomeXchange посредством базы данных PRIDE (PRoteomics IDEntifications) [49] с идентификатором набора данных PXD029188.
Статистический анализ
Все статистические анализы проводились с использованием ПО R версии 4.1.0. Демографические и клинические данные субъектов сравнивались с использованием однофакторного дисперсионного анализа, критерия Крускала – Уоллиса и критерия хи-квадрат для непрерывных, порядковых и категориальных типов данных соответственно. Для нормализации данных количественного определения белка применяли log2-трансформацию и нормализацию медианы. Для сравнительного анализа содержания белка при статистическом тестировании использовались только белки, идентифицированные более чем в 80 % образцов. Анализ на уровне белка проводили с использованием эмпирических байесовских модерируемых тестов, реализованных в программном пакете R/Bioconductor limma [50]. В частности, метод Limma использует подход линейной модели для анализа экспрессии генов или содержания белка в ковариатах. В отличие от обычной линейной модели, основанной на методе наименьших квадратов, для подгонки модели к уровню экспрессии отдельного белка Limma использует эмпирический байесовский подход. Сила разных белков берется для оценки среднего значения и дисперсии содержания белка, проверки контраста параметров модели, представляющих научный интерес. P-уровни модерируемого t-теста нескольких белков дополнительно корректируются с использованием метода частоты ложных результатов Бенджамини – Хохберга. Таким образом, статистический метод Limma позволяет справиться с трудностями, характерными для небольшой выборки; он отличается высокой точностью и используется для сравнительного анализа протеомных данных [51]. Статистически значимыми считались только белки со скорректированным p-уровнем ниже порога (альфа = 0,05) и кратным изменением содержания ≥ 2 (абсолютное значение log2 (кратное изменение) ≥ 1). Уникальными считались белки, имеющиеся во всех образцах одной группы, но не присутствующие ни в одной другой группе. Были классифицированы термины биологического процесса генной онтологии (ГО), связанные с идентифицированными белками; анализ обогащения выполнялся с использованием программного пакета Rgprofiler2 [52]. В частности, с его помощью реализован кумулятивный гипергеометрический тест для анализа обогащения с использованием метода g:Profiler. При данном методе проводится коррекция нескольких тестов, чтобы уменьшить количество ложноположительных результатов. Учитывается перекрытие функциональных терминов и взаимозависимость тестов. Следовательно, этот метод более консервативный по сравнению с методом Бенджамини – Хохберга и менее ограничивающий, чем метод поправки Бонферрони. g:Profiler сообщает о скорректированных значениях p-обогащения. Классификация белков и анализ путей роста белковых структур проводились с использованием системы классификации PANTHER (анализ белков через эволюционные отношения) [53, 54]. PANTHER в качестве алгоритма по умолчанию реализует точный тест Фишера с коррекцией частоты ложных результатов Бенджамини – Хохберга для множественного тестирования.
Результаты
Демографические и клинические характеристики лиц, участвовавших в исследовании
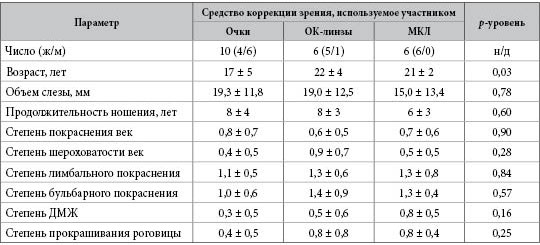
Демографические данные и характеристики поверхности глаз пользователей очков, ОК-линз и МКЛ показаны в табл. 1. В группе участников, носящих очки, был более широкий возрастной диапазон, и они были примерно на 4–5 лет моложе, чем респонденты, использующие ОК-линзы (p = 0,04), но достоверных отличий от пользователей МКЛ нет (p = 0,08). В целом, результаты обследования с помощью щелевой лампы были в ожидаемых пределах нормы для детей и молодых людей, носящих очки и КЛ. Не наблюдалось никаких существенных различий между группами по продолжительности использования, секреции слезы, покраснению и шероховатости век, состоянию сосочков, лимбальному и бульбарному покраснению, ДМЖ или окрашиванию роговицы.
Таблица 1
Демографические и клинические характеристики участников исследования
Данные протеомики
Количество белковых групп, идентифицированных у каждого субъекта, варьировало от 889 до 3082 (рис. 1а), что свидетельствует о неоднородности состава слезного протеома у разных людей. Распределение содержания белка и графики анализа основных компонентов показаны на рисунках S1 и 2, которые можно найти в дополнительных материалах. Среднее количество белковых групп, идентифицированных в каждой группе оптической коррекции, составляло 1978 для очков, 1756 для ОК-линз и 2009 для пользователей МКЛ (обозначены черными полосами на рис. 1а). Не было никаких существенных различий между всеми тремя группами в количестве идентифицированных белков. Всего было идентифицировано 3206, 3139 и 3134 белковых групп в группах с очками, ОК-линзами и МКЛ соответственно. Во всех трех группах идентифицировано 3406 белковых групп – самое большее количество белков, идентифицированных в образцах слезных полосок Ширмера. Классификация, основанная на категориях генной онтологии, показана в дополнительном материале на рис. S3. 2910 групп белков были идентифицированы как минимум в одном образце из каждой корректирующей группы, что составляет 85,4 % от общего количества белков, идентифицированных в этом исследовании (рис. 1б). Высокое перекрытие между различными группами оптической коррекции указывает на то, что состав слезного протеома в них был одинаковым.
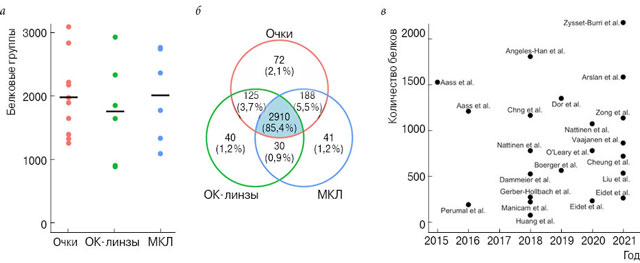
Рис. 1. а – количество белковых групп, идентифицированных у каждого участника, носящего очки, ОК-линзы или МКЛ (черные линии показывают среднее количество белковых групп); б – диаграмма Венна, которая показывает перекрытие и уникальность идентифицированных белков в каждой группе участников; в – количество белков в слезе, выделенной из полосок Ширмера, судя по научным публикациям с 2015 по 2021 год
Влияние типа линзы на протеом слезы
В общей сложности были идентифицированы и использованы для статистического анализа 925 белков в > 80 % образцов слезы всех 22 участников. Не было существенных различий по содержанию белка ни между участниками, использующими очки и ОК-линзы, ни между участниками, которые носят очки и МКЛ (рис. 2а, б). У участников, носящих МКЛ и ОК-линзы, после учета поправки на возраст было обнаружено, что 19 групп белков по-разному экспрессировались (рис. 2в). Из них 8 белковых групп были активизированы, а 11 – подавлены у участников, применяющих МКЛ, если сравнивать их с теми, кто использует ОК-линзы. Эти белки были разделены на пять категорий по классификации PANTHER. Для каждой категории показано количество белков с повышенной и пониженной экспрессией в группе пользователей МКЛ (рис. 2г). В табл. 2 перечислены идентификаторы UniProt ID, гены и названия этих 19 групп белков, их классы. Все защитные иммунные белки, такие как тяжелый вариабельный домен иммуноглобулина 1–46 (IGHV1–46), были усилены в группе участников, носящих МКЛ, по сравнению с теми, кто использует ОК-линзы. Все четыре фермента взаимопревращения метаболитов, такие как, например, фактор торможения миграции макрофагов (MIF), были снижены в группе использующих МКЛ по сравнению с теми, кто носит ОК-линзы. На рис. 2д показано, что многие белки участвуют в сигнальных, иммунных и воспалительных реакциях. Полный список идентификаторов генной онтологии и терминов включен в таблицу дополнительных материалов S1.
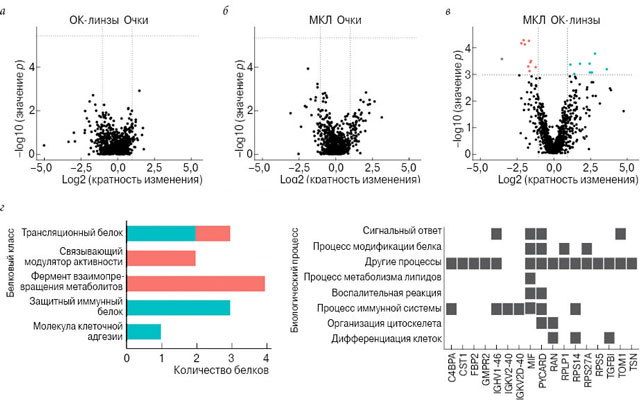
Рис. 2. а–в – графики рассеяния, показывающие сравнительное содержание белка в группах участников, использующих ОК-линзы и очки, МКЛ и очки, МКЛ и ОК-линзы соответственно. Пунктирными линиями обозначены пороговые значения p после нескольких корректировок тестирования и кратного изменения содержания белка; г – классификация белков, дифференциально экспрессируемых в группах участников, носящих МКЛ и ОК-линзы (![]() – ниже,
– ниже, ![]() – выше); д – генные онтологические биопроцессы с участием белков, дифференциально экспрессируемых в группах пользователей МКЛ и ОК-линз
– выше); д – генные онтологические биопроцессы с участием белков, дифференциально экспрессируемых в группах пользователей МКЛ и ОК-линз
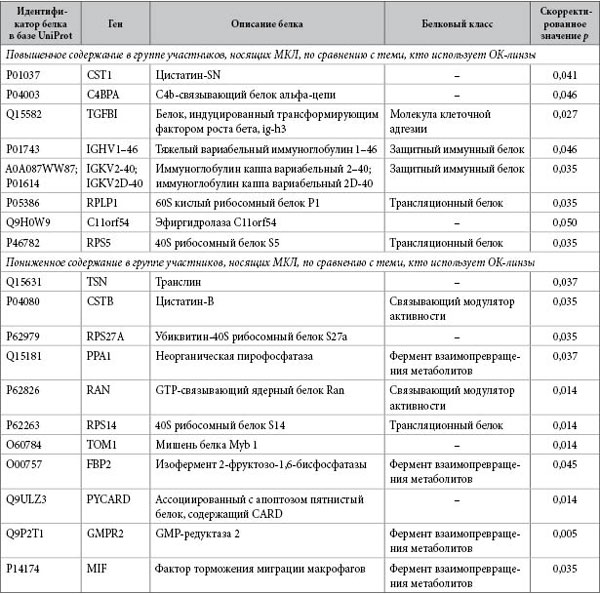
Таблица 2
Список групп белков, в котором показано их различное содержание в группах пользователей МКЛ и ОК-линз, а также классификация PANTHER
Влияние возраста на протеомы слезы
Чтобы оценить влияние возраста на белковый состав, использовались профили протеома слезы носителей очков. Лиц моложе 18 лет отнесли к категории детей (n = 5), а лиц от 18 лет и старше – ко взрослым (n = 5). Выяснилось, что содержание 82 групп белков отличается: 67 из них у детей встречаются чаще, а 15 – реже, если сравнивать с молодыми взрослыми (рис. 3а). Анализ обогащения генной онтологии показал 18 обогащенных биологических процессов с участием 82 белков, в том числе 25 белков, участвующих в защитном ответе (GO:0006952), 15 – в ответе врожденного иммунитета (GO:0045087), 14 – в воспалительном ответе (GO:0006954), и 9 – в процессе метаболизма гликопротеинов (GO:0009100) (рис. 3б). Полный список дифференциально экспрессируемых белков и связанных с ними идентификаторов генной онтологии и терминов включен в таблицы дополнительных материалов S2 и 3. Кроме того, мы разделили эти 82 группы белков на 12 классов белков PANTHER; для каждой категории показано количество белков с повышенной и пониженной экспрессией у детей (рис. 3в). Четыре белка являются защитными/иммунными; из них три белка активизированы [иммуноглобулин с тяжелой константой гамма-4 (IGHG4), богатый цистеином секреторный белок-3 (CRISP3) и бета-2-микроглобулин (B2M)], а один [тяжелый вариабельный иммуноглобулин 1–45 (IGHV1–45)] снижен у детей по сравнению со взрослыми. У детей повышалась активность всех пяти межклеточных сигнальных молекул, включая хемокины 10 (CXCL10) и 17 (CXCL17) с C-X-C-мотивом. Из 18 ферментов взаимопревращения метаболитов содержание 12 у детей было повышено – например, полипептидов N-ацетилгалактозаминилтрансферазы 3 и 5 (GALNT3 и GALNT5), CMP-N-ацетилнейраминатин-бета-галактозамид-альфа-2,3-сиалилтрансферазы 1 (ST3GAL1) и бета-1,4-галактозилтрансферазы 1 (B4GALT1). Напротив, шесть ферментов, в том числе MIF, были подавлены у детей по сравнению с молодыми людьми.
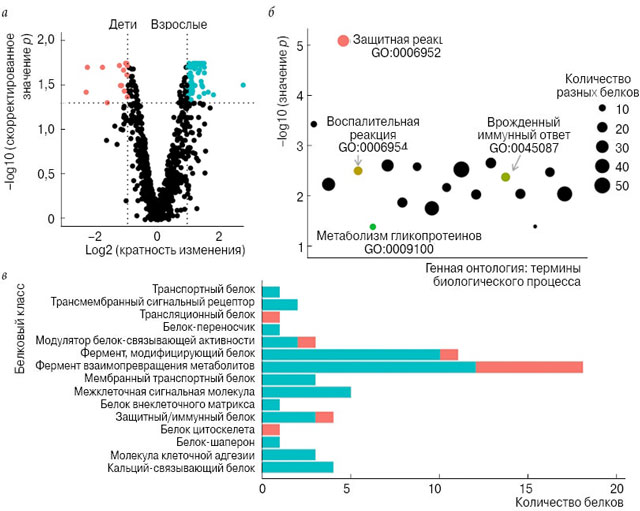
Рис. 3. а – график рассеяния содержания белка у взрослых и детей; б – анализ обогащения генной онтологии дифференциально экспрессируемых белков. Бóльший размер круга означает бóльшее количество белков в термине; в – классификация дифференциально экспрессируемых белков у взрослых и детей (![]() – ниже,
– ниже, ![]() – выше)
– выше)
Обсуждение
Протеомика на основе масс-спектрометрии широко использовалась для обнаружения биомаркеров и проверки результатов клинических исследований, потому что она дает огромные возможности глубокой характеризации сложных протеомов. Такие исследования часто требуют беспристрастных методов, комплексных и количественных [35, 40, 55]. При использовании технологии, основанной на DDA, для фрагментации отбираются ионы-предшественники. Поэтому, если содержание белка низкое, DDA часто дает плохо воспроизводимые результаты при идентификации и количественном определении белка. При использовании DIA на фрагментацию отправляются все ионы в каждом заранее заданном диапазоне масс. Поэтому с помощью данной технологии можно получить более полные и воспроизводимые результаты, и она идеально подходит для клинических исследований с большой выборкой [40]. К тому же при подходе PASEF ионы сначала накапливаются, а затем высвобождаются в зависимости от их подвижности, что значительно повышает чувствительность обнаружения [36, 43, 44].
В этой работе мы использовали подход diaPASEF и распознали в среднем около 2 тыс. белков за один проход, в общей сложности 3406 белковых групп – на сегодняшний день это наибольшее количество белков, идентифицированных в слезе. Сведения о белках в слезе человека, идентифицированных с помощью полосок Ширмера, опубликованные в литературе с 2015 по 2021 год [16, 20, 56–78], показывают, что ранее регистрировалось самое большее 2172 белка [78] (см. рис. 1в). Следует отметить, что во многих исследованиях сообщается количество не всех идентифицированных белков, а только тех, которые имеют значительные изменения. Поэтому такие исследования мы не учитываем. Большой разброс в количестве идентифицированных белков в опубликованной литературе (от нескольких сотен до более чем 2 тыс.) может быть связан с несколькими причинами. В их числе – условия жидкостной хроматографии и разделение образца на несколько фракций, что значительно увеличивает количество идентифицированных белков.
Применение инструментов технологии «омик» на основе масс-спектрометрии для изучения миопии было обобщено в обзорной статье Гроховски (Grochowski) и соавторов [79]. Однако пока недостаточно исследований молодых пациентов с миопией, несмотря на тот факт, что осложнения, связанные с КЛ, наиболее часты у пациентов в возрасте 15–25 лет [8–11]. В этом исследовании мы профилировали протеомы слезы у лиц в возрасте от 10 до 26 лет, которые носили очки, ОК-линзы или МКЛ более 3 лет. У этих пациентов не было активного воспаления поверхности глаза, поэтому они считались «здоровыми» пользователями. Содержание белка в слезе в группах тех, кто носил ОК-линзы и очки или МКЛ и очки, существенно не различалось. Этот вывод противоречит нескольким опубликованным исследованиям [20, 80]. Помимо прочего, это может объясняться популяционной выборкой (например, возрастной группой), состоянием здоровья поверхности глаза, методами сбора образцов и статистического анализа. Влияние возраста и метода сбора образцов на протеомы слезы будет обсуждаться далее. С учетом возраста у пользователей МКЛ и ОК-линз было выявлено 19 групп дифференциально экспрессируемых белков.
Из 19 групп белков, которые различались у участников, носящих МКЛ и ОК-линзы, ряд из них вызван воспалением и иммунитетом. Это белки, связанные с апоптозом, пятнистые белки, содержащие CARD (PYCARD), MIF и IGHV1-46. Белок PYCARD является частью инфламмасомного полимерного комплекса – белка-3 (NLRP3), содержащего домены NACHT, LRR и PYD [81]. Инфламмасома играет ключевую роль в воспалении и врожденном иммунитете. Она опосредует процессинг и секрецию провоспалительных цитокинов интерлейкина-1β (IL1β) и IL18 в ответ на инфекцию и повреждение клеток [81]. Сообщалось об активации инфламмасомы NLRP3 в слезах пациентов с синдромом сухого глаза (ССГ) [82]. Белок MIF является провоспалительным цитокином [83], необходимым для сборки и активации воспалительных процессов NLRP3, а ингибирование MIF подавляет NLRP3-зависимую секрецию IL1β и IL18 [84]. Ранее сообщалось о белке IGHV1-46 в слезах пациентов с ССГ, было предложено считать его биомаркером воспаления поверхности глаза [85]. В данном исследовании изменение количества PYCARD, MIF и IGHV1-46 у пользователей ОК-линз по сравнению с теми, кто носит МКЛ, предполагает различные глазные иммунные/воспалительные реакции. Кроме того, ингибиторы протеазы цистатин-B (CSTB) и цистатин-SN (CST1) также по-разному экспрессировались у участников, использующих МКЛ и ОК-линзы. Ингибиторы протеазы особенно важны для поддержания тканевого гомеостаза. Белок CSTB был обнаружен в слезной пленке [86, 87], и его содержание было повышенным при ношении жестких КЛ по сравнению с МКЛ [20]. Это согласуется с нашими выводами.
Итак, в данном исследовании идентифицированы несколько белков, содержание которых в слезной пленке молодых пациентов существенно повышается в ответ на ношение КЛ. Эти белки могут играть роль в воспалении глаз и поддержании глазного гомеостаза. Все участники исследования были молодыми людьми, которые постоянно носили КЛ (более 3 лет) и не имели активных глазных осложнений. Поэтому разница в содержании белка может указывать на адаптацию глаз к ношению мягких и жестких КЛ. В будущем необходимы проспективные исследования для изучения потенциальных связей между этими белками и осложнениями, вызванными ношением КЛ.
Чтобы понять, как возраст влияет на протеомы слезы, мы разделили группу пользователей очков на детей и взрослых и обнаружили, что 82 белка в этих двух подгруппах экспрессируются по-разному. Многие из них связаны с воспалением и иммунитетом, такие как CXCL10, CXCL17, PYCARD, MIF, IL18 и SERPINA3. Белок CXCL10, провоспалительный цитокин, используется клетками роговицы для связи с нейтрофилами [87] и участвует в воспалении и инфекции глаз [88–89]. Его содержание повышается в слезах пациентов с острым фолликулярным конъюнктивитом [90]; он рассматривался как предполагаемый биомаркер ССГ [70, 91–94]. В целом, очевидно, что белок CXCL10 участвует в воспалительных заболеваниях глаз. Белок CXCL17, хемокин слизистых оболочек, действует как ингибитор воспаления, поддерживающий иммунный гомеостаз при воспалительных состояниях [95-98]. Как CXCL10, так и CXCL17 были сверхэкспрессированы у детей по сравнению с молодыми людьми. IL18 представляет собой провоспалительный цитокин, высвобождаемый при активации инфламмасомы NLRP3 [99]. Вместе с MIF и PYCARD, как описано выше, они участвуют в воспалении глаз и иммунитете. SERPINA3 – это белок, отвечающий за опосредование воспалительных реакций, и его активация может быть признаком повышенного уровня воспаления глаз [29, 64, 100]. В данном исследовании эти белки по-разному экспрессировались у детей и молодых людей, что свидетельствует о различиях в воспалениях глазной поверхности и иммунных состояниях.
Среди белков, по-разному экспрессируемых у детей и молодых взрослых, есть многие ферменты взаимопревращения метаболитов, участвующие в синтезе и деградации муцинов и других типов гликанов. Гликаны и гликоконъюгаты отвечают за целостность поверхности глаза и регулируют ее взаимодействие с внешней средой [101–103]. Поэтому предполагается, что изменение количества этих ферментов является индикатором заболеваний глазной поверхности [104–105]. GALNT3 и GALNT5, ST3GAL1 и B4GALT1 участвуют в синтезе муциновых гликанов О-типа на поверхности глаза [106–109]. Заболевания глаз, такие как глазной рубцовый пемфигоид, изменяют распределение гликозилтрансфераз GALNT, и по мере прогрессирования заболевания экспрессия ферментов GALNT может быть утрачена [106]. Нейтральная альфа-глюкозидаза AB (GANAB), альфа-1,3-маннозилгликопротеин 2-бета-N-ацетилглюкозаминилтрансфераза (MGAT1) и альфа-N-ацетилглюкозаминидаза (NAGLU) участвуют в биосинтезе N-гликанов. Снижение активности GANAB в слезах пациентов с ССГ указывает на нарушение функции глазного барьера [29]. Резкое снижение содержания MGAT1 вызывает частичную потерю другого белка MUC16 (как в целом, так и на клеточной поверхности) и сопутствующее снижение барьерной функции гликокаликса [110]. Белки альфа-субъединица бета-гексозаминидазы (HEXA) и NAGLU участвуют в деградации гликозаминогликанов. HEXA и галектин-3-связывающий белок (LGALS3BP) были подавлены в слезах пациентов с ССГ [111], что указывает на нарушение функции глазного барьера. Все эти белки вносят свой вклад в поддержание гомеостаза поверхности глаза. В текущем исследовании они по-разному экспрессировались в слезах детей и молодых людей, что указывает на разный гомеостаз поверхности глаза в этих возрастных группах. Ношение КЛ отрицательно влияет на плотность муцина на поверхности глаза [112]. Поэтому возникает соблазн предположить, что эти белки, участвующие в синтезе и деградации гликанов на поверхности глаза, способствуют его возрастным реакциям на ношение КЛ.
Известно, что старение влияет на все отделы глаза [113–123]. В недавнем исследовании Нэттинен (Nättinen) и соавторы [124] идентифицировали 17 белков слезы, достоверно коррелирующих с возрастом. Многие из них связаны с воспалением, иммунным ответом и гибелью клеток, что согласуется с нашими выводами. Белок маммаглобин-А (SCGB2A2) обычно идентифицируется как по-разному экспрессируемый в цитируемом и нашем исследованиях. SCGB2A2 положительно коррелировал с увеличением возраста [124], что согласуется с нашими выводами. Тем не менее идентификация большого количества неперекрывающихся белков в этих двух исследованиях может быть связана с целым рядом факторов: состоянием здоровья глаз (после глазной операции по сравнению со здоровыми глазами без хирургии в анамнезе), возрастом пациента (взрослые от 18 до 83 лет; дети и молодые люди от 10 до 26 лет), методом сбора слезы (микрокапиллярные трубки или полоски Ширмера). Метод сбора слезы влияет на состав протеома слезы и содержание белков, что дополнительно обсуждается далее.
У нашего исследования есть ряд ограничений. Гендерный состав не сбалансирован, большинство испытуемых были женщинами. Лица моложе 18 лет оценивались только в группе пользователей очков, размер выборки был небольшим. Кроме того, вызывает беспокойство относительно большое временнóе окно сбора образцов: возможно, изменчивость протеома вызвана циркадными колебаниями (есть подобные сообщения о белках в слюне [125–126]). Метод сбора слезы может влиять на состав и содержание белков [73, 127]. Из-за контакта полоски Ширмера с поверхностью глаза в образец слезы могут попасть глазные клетки. Сравнение результатов разных исследований бывает проблематичным из-за того, что собиралась слеза разного типа (рефлекторная или базальная). Несмотря на эти ограничения, наше открытие привлекает внимание к возрастным различиям протеома поверхности глаза, особенно у детей. Кроме того, программа Skyline помогла обнаружить, что большинство дифференциально экспрессируемых белков (54 из 82) значительно различаются у детей и молодых людей. У них самый высокий риск развития осложнений, вызванных КЛ. Вероятно, что реакция глаз на КЛ в этих двух группах будет отличаться. Поэтому необходимы дальнейшие исследования среди детей – пользователей КЛ.
Заключение
Используя подход diaPASEF, мы идентифицировали 3406 белков в образцах слезы, собранных с помощью полосок Ширмера. Выяснилось, что содержание 19 белковых групп значительно отличалось в группе пользователей МКЛ по сравнению теми, кто применяет OK-линзы. Содержание в слезе 82 белков отличалось у детей и молодых людей, использующих очки. Наличие многих важных белков связано с воспалением и иммунитетом, а также с гомеостазом поверхности глаза. В целом, данное исследование дает глубокий охват протеома слезы и предполагает необходимость изучения реакции глаз на ношение КЛ отдельно для подростков и молодых людей.
Авторы исследования: Готин Цинь (Guoting Qin), Колледж оптометрии при Хьюстонском университете (Хьюстон, США), Лаборатория масс-спектрометрии, химический факультет, Хьюстонский университет (Хьюстон, США); Сесилия Чао (Cecilia Chao), Колледж оптометрии при Хьюстонском университете (Хьюстон, США), Школа оптометрии и науки о зрении, Университет Нового Южного Уэльса (Сидней, Австралия); Лорен Дж. Лэттери (Lauren J. Lattery), Колледж оптометрии при Хьюстонском университете (Хьюстон, США); Хун Линь (Hong Lin), факультет компьютерных наук и инженерных технологий, Хьюстонский университет (Хьюстон, США); Вэньцзян Фу (Wenjiang Fu), факультет математики, Хьюстонский университет (Хьюстон, США); Кэтрин Ричдейл (Kathryn Richdale), Колледж оптометрии при Хьюстонском университете (Хьюстон, США); Чэнчжи Цай (Chengzhi Cai), Лаборатория масс-спектрометрии, химический факультет, Хьюстонский университет (Хьюстон, США).
Перевод: Н. Вахтина
Статья опубликована на сайте ScienceDirect 01.10.22. Печатная публикация статьи запланирована к выходу в журнале Journal of Proteomics 06.01.2023. © 2022 Elsevier B.V. All rights reserved
© РА «Веко»
Печатная версия статьи опубликована в журнале «Современная оптометрия» [2022. № 9 (158)].
По вопросам приобретения журналов и оформления подписки обращайтесь в отдел продаж РА «Веко»:
- Тел.: (812) 634-43-34.
- E-mail: magazine@veko.ru
- veko.ru
Наши страницы в соцсетях:
.jpg)











